白晨教授与深圳大学附属华南医院合作在Membranes杂志发文
July 7, 2022

膜蛋白在跨膜分子运输、细胞通信和信号转导等生理活动中发挥重要作用。现今药物市场中,超过60%的上市药物其靶标属于膜蛋白家族。因而对膜蛋白工作机制的深入了解是具有重要的科学意义和应用价值。但由于膜结构难以解析以及蛋白质结构空间尺度较大,在很大程度上制约着对膜蛋白工作机理的研究。
白晨教授与深圳大学华南附属医院吴松院长合作,在Membranes发表文章——Mechanism Study Of Proteins Under Membrane Environment,从动力学角度揭示了三种具有代表性膜蛋白(TMEM16A氯离子通道、C类GPCR受体mGlu2、磷脂转运蛋白P4-ATPase)的工作机理。
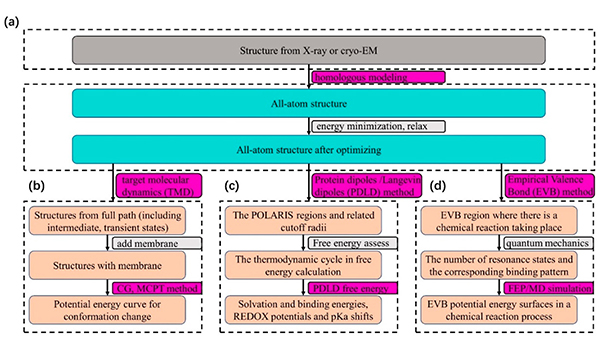
在这项工作中,白晨教授采用2013年诺奖得主Arieh Warshel长期开发的CG模型探索这三种代表性膜蛋白系统的工作过程。通过计算动力学过程的自由能分布和反应能垒,确定最佳反应路径。这套CG模型可准确描述生物大分子体系的静电作用和可电离残基的溶剂化作用,在大尺度生物体系模拟中具有有力的优势。当前工作为TMEM16A通道激活、mGlu2受体激活过程以及P4-ATPase酶磷脂转运过程提供了合理的解释。尽管三种系统均属于膜蛋白家族成员,但其在工作过程的能量表现截然不同。
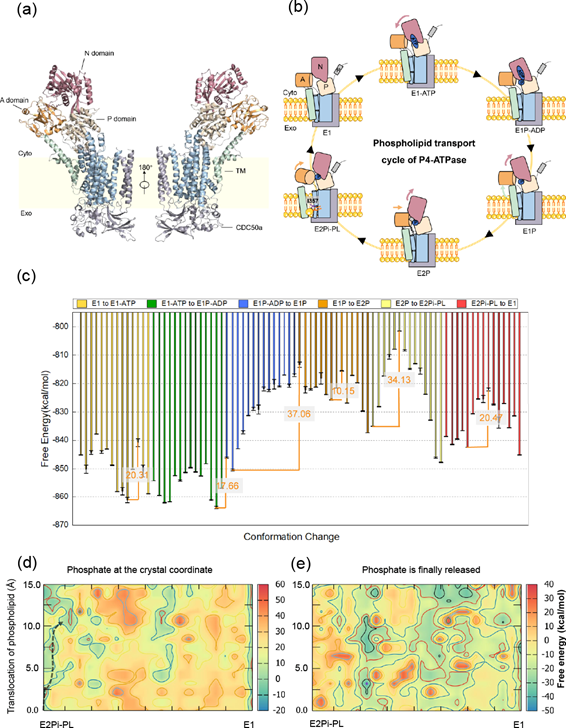
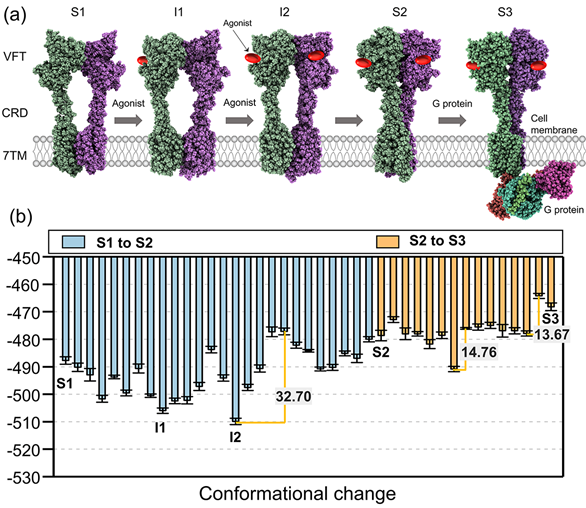
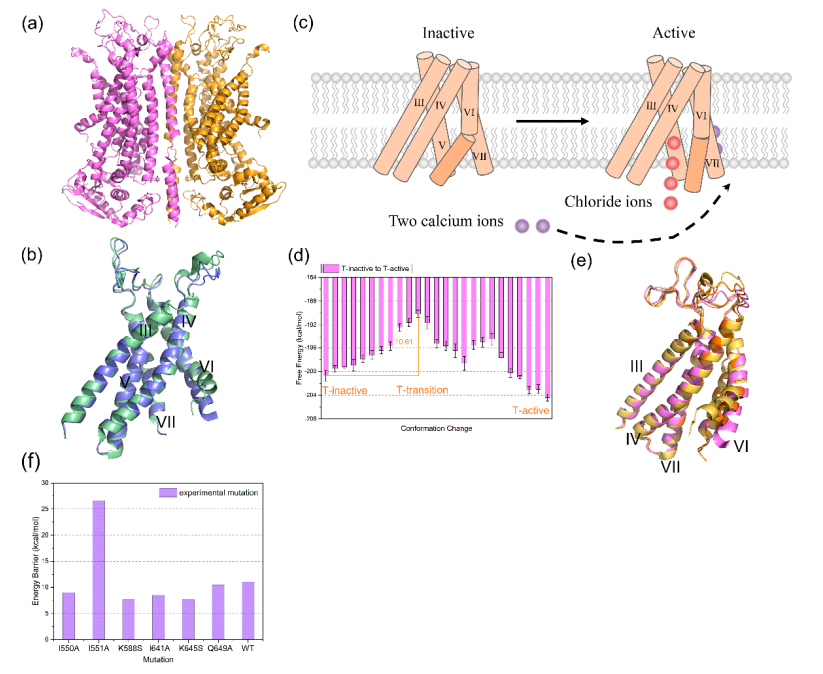
此外,高速原子力显微镜与CG模型的结合使用,有助于科研工作者在原子层面从结构和能量角度进一步阐明与构象变化相关的分子机制,突破当前膜蛋白分子机制研究领域的瓶颈。